Os átomos se ligam entre si para formar as moléculas. Os tipos de ligação são:
Regra do octeto: A partir da observação dos gases nobres que possuem 8 elétrons em sua última camada (com exceção do Hélio que possui 2 elétrons), formulou-se a regra de que os átomos se estabilizam eletronicamente quando atingem esse valor. Essa regra não abrange todos os casos de ligações atômicas, mas auxilia preliminarmente no estudo do assunto.
- Ligação iônica ou eletrovalente
- Ligação covalente ou molecular
- Ligação covalente dativa ou coordenada
- Ligação metálica
Ligação Iônica
Ligação entre íons, de natureza eletromagnética

Exemplo: NaCl → cloreto de sódio (sal de cozinha)
Obs.: Íons são átomos que possuem uma carga elétrica por adição ou perda de um ou mais elétrons.
Na ligação iônica o resultado final é eletricamente neutro.
Na fórmula dos compostos iônicos a quantidade de elétrons cedidos é igual à quantidade de elétrons recebidos.
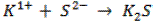
Uma regra prática é que os coeficientes da fórmula final sejam o inverso dos índices de carga elétrica.
Normalmente os elementos que se ligam ironicamente são os das famílias IA, IIA e IIIA com os das famílias VA, VIA e VIIA da tabela periódica.
Ligação Covalente ou Molecular
Ligação em que pares de elétrons são compartilhados pelos núcleos. Sendo que um elétron de cada par é cedido por cada um dos núcleos.

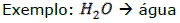
Uma maneira de apresentar uma molécula de substância covalente é a fórmula estrutural plana, ou de Couper:
H – O – H
Cuja fórmula molecular é: 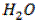
Cada traço representa um par de elétrons compartilhados.
Obs.: como não há nem perda nem ganho de elétrons a molécula formada é eletricamente neutra.
Normalmente os elementos que se ligam por covalência são os das famílias VA, VIA, VIIA e IVA tabela periódica e, eventualmente, o elemento Hidrogênio.
Ligação Covalente dativa ou Coordenada
Essa ligação é semelhante a molecular, com a diferença de que só um dos núcleos cede o par de elétrons compartilhados.
Obs.: dessa maneira os núcleos estão estabilizados eletronicamente.
Exemplo: O = S → O
Ligações Metálicas Como os metais possuem a tendência de formar cátions pela cessão de elétrons, esses cátions formam um retículo cristalino envolto em uma nuvem eletrônica.

Exemplo: Ferro (Fe), Alumínio (Al), Cobre (Cu).
Exercícios:

a. Em que grupo da Tabela Periódica estariam os elementos X e Y?
b. Consulte a Tabela Periódica e dê o símbolo de dois elementos que poderiam corresponder a X e a Y
(Unicamp) Considerando os elementos sódio (Na), magnésio (Mg), enxofre (S) e cloro (Cl), escreva as fórmulas dos compostos iónicos que podem ser formados entre eles.
(UEL) A melhor representação para a fórmula estrutural da molécula de dióxido de carbono é:
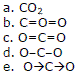

a. Represente a configuração eletrônica desse elemento.
b. A que família pertence?
(Dados os números atômicos: H=1 e Na=11)
Respostas:
1)
a. X grupo IA (metal alcalino) e Y grupo IIA (metal alcalino terroso).
b. podem ser vários pares entre eles X=Na e Y=Mg.
2)
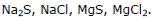
3) c.
4)
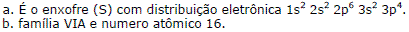


 “Murcha” ou “mucha”: qual é o certo?
“Murcha” ou “mucha”: qual é o certo? “Seriguela” ou “ciriguela”: qual o certo?
“Seriguela” ou “ciriguela”: qual o certo? “Guerra Civil”: o que o filme com Wagner Moura ensina sobre História e política
“Guerra Civil”: o que o filme com Wagner Moura ensina sobre História e política Participantes do Pé-de-Meia podem fazer o Enem de graça – e ainda receber por isso
Participantes do Pé-de-Meia podem fazer o Enem de graça – e ainda receber por isso Filmes que você não sabia mas são inspirados em Shakespeare
Filmes que você não sabia mas são inspirados em Shakespeare