Matéria e energia: Reações de oxirredução

ENERGIA À MÃO A bateria dos celulares é um dispositivo que transforma energia química em energia elétrica
Usinas portáteis
A energia elétrica de pilhas e baterias vem da transferência de elétrons que ocorre numa reação química
A energia elétrica que abastece a maioria das residências no Brasil vem das usinas hidrelétricas, por meio de fios. Mas a eletricidade pode ser gerada e usada sem os fios de transmissão, em pilhas e baterias. Esses dispositivos, que transformam energia química em energia elétrica, são fundamentais para tecnologias utilizadas em celulares, notebooks e aparelhos de MP3.
PILHAS E BATERIAS
São dispositivos de mesma natureza. A diferença é que a bateria reúne uma série de pilhas.
Oxirredução
As pilhas e baterias convertem em energia elétrica a energia química de substâncias em seu interior, por meio de uma reação de oxirredução ou de oxidação-redução, em que espécies químicas transferem elétrons de uns para outros. Nas reações por transferência de elétrons, a espécie química que doa elétrons é o agente redutor, que sofre oxidação. A espécie que recebe elétrons é o agente oxidante (espécie que sofre redução e gera a oxidação da outra espécie). Mantenha em mente:
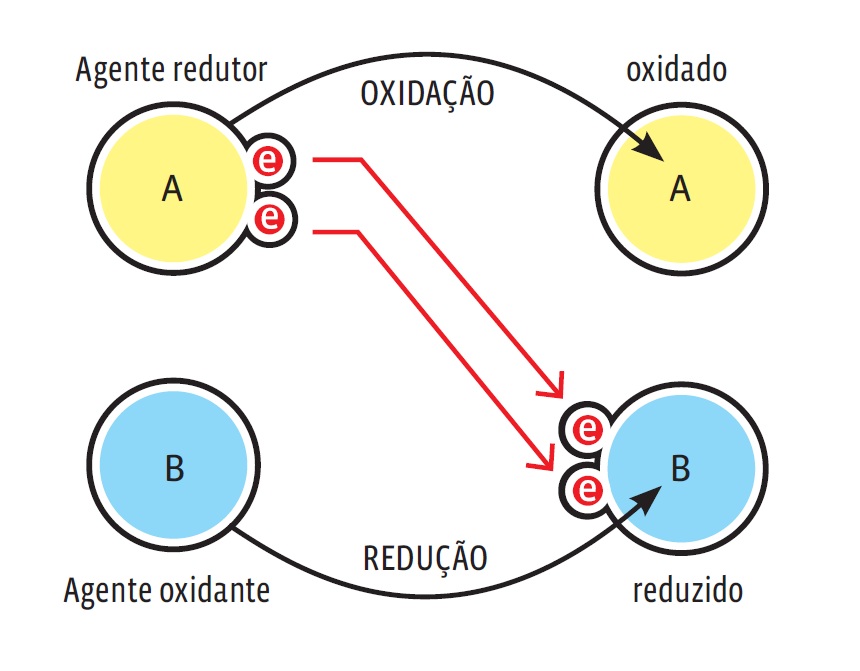
QUEM DÁ, QUEM TIRA A perde elétrons e, portanto, é oxidada por um agente oxidante (B). A substância B, por outro lado, sofre redução porque recebe os elétrons cedidos por A, que é o agente redutor.
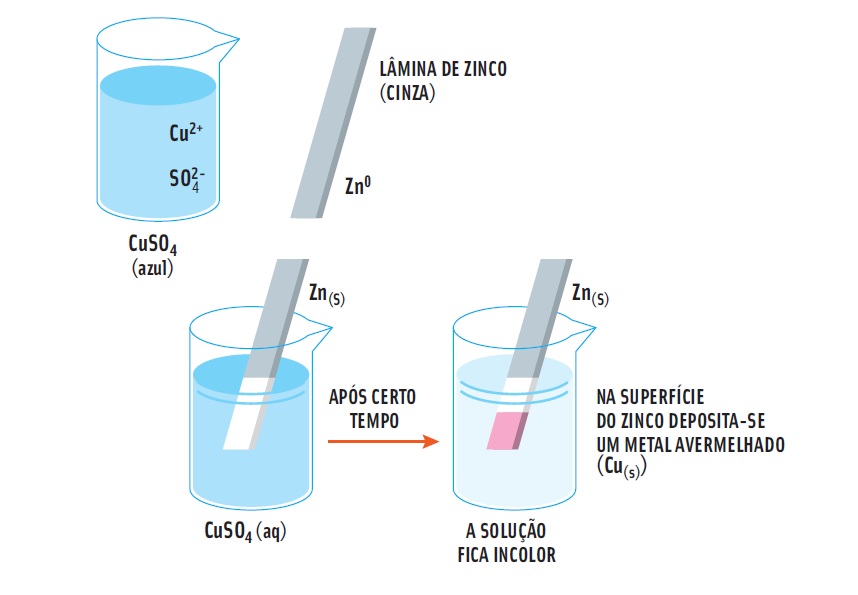
Acompanhe o raciocínio no exemplo a seguir de uma reação de oxirredução do zinco metálico (na placa) e uma solução de sulfato de cobre:
ESPÉCIE QUÍMICA
É a expressão genérica a átomos,íons e moléculas.
- • Na placa, os átomos de zinco (Zn) estão unidos por ligações metálicas.
- • Já no sulfato de cobre (CuSO4), que é um sal, os átomos se mantêm coesos por ligações iônicas. O sulfato de cobre está dissolvido em água (H2O).
- • Em solução, as moléculas H2O separam os íons do CuSO4: de um lado, os cátions de cobre (Cu2+), de outro, os ânions de sulfato (SO4 2-).
- • Agora entra o zinco: a reação entre Zn e o sulfato de cobre libera na solução de íons Zn2+.
- • O cobre metálico fica depositado sobre a placa de zinco. A equação química que representa esse processo é: Zn + Cu2+ → Zn2+ + Cu
- • Nessa reação, o zinco transferiu elétrons para o íon Cu2+. O zinco, então, que doou elétrons, sofreu oxidação, e o íon cobre, que recebeu elétrons, sofreu redução. Daí o nome reação de oxirredução. Essa reação pode ser entendida em duas etapas sequenciais:
- • Oxidação do Zn, que doa dois elétrons e se transforma num cátion: Zn → Zn2+ + 2 e–
- • Redução do cátion Cu2+, que recebe os dois elétrons cedidos por Zn: Cu2+ + 2 e– → Cu

Pilhas
Você viu: na reação entre a placa de zinco e o sulfato de cobre, o zinco se oxida ao doar elétrons aos cátions de cobre soltos na solução. Por sua vez, os cátions de cobre que recebem os elétrons do zinco se depositam como cobre metálico na superfície da placa de zinco. Uma pilha nada mais é do que um dispositivo em que essa transferência de elétrons ocorre de maneira ordenada, ao longo de um fio, que conecta os dois metais. O inglês John Frederic Daniell construiu uma pilha eficiente. Veja:
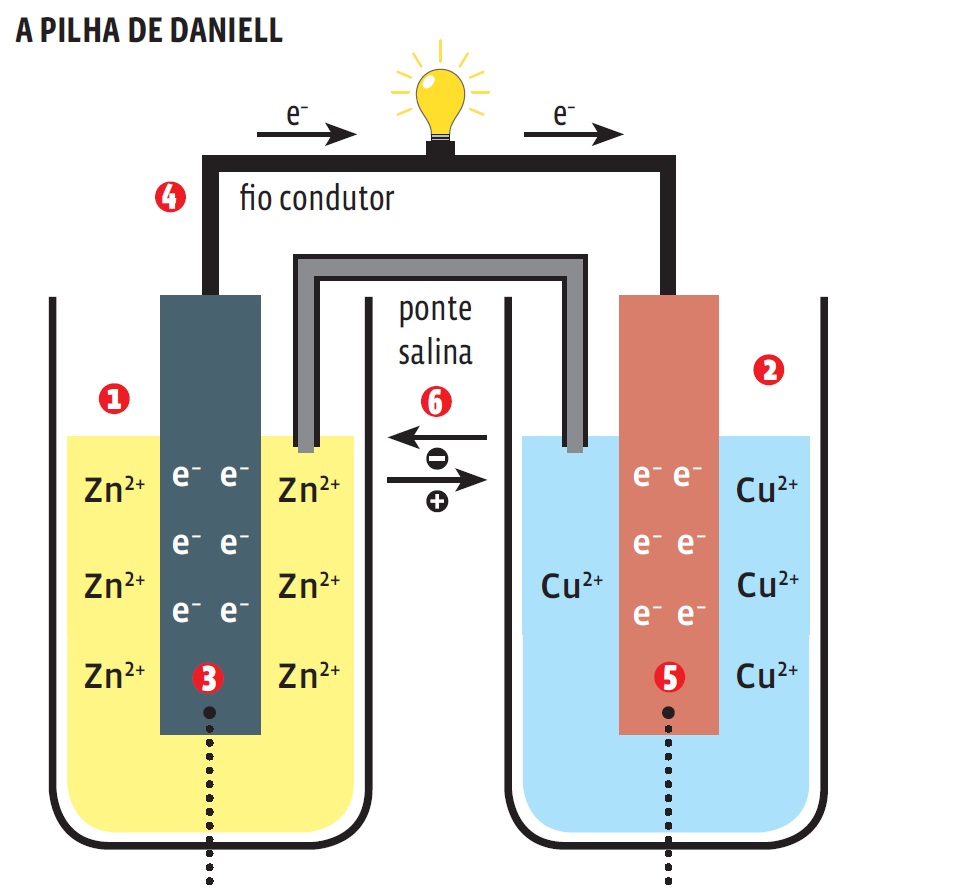
1. Uma barra de zinco foi mergulhada numa solução de sulfato de zinco, carregada de íons de zinco. Esse é o eletrodo de zinco.
2. Outra barra, de cobre, foi mergulhada numa solução de sulfato de cobre, que contém íons de cobre. Esse é o eletrodo de cobre.
3. Como o zinco tem maior tendência a se oxidar (a perder elétrons), a barra solta na solução íons Zn2+. Ficam na placa os elétrons que foram abandonados (e–). O zinco sofre oxidação e se torna o polo negativo da pilha, ou anodo.
4. Um fio condutor faz com que os elétrons cedidos pelo zinco cheguem à barra de cobre. Se o fio passar por uma lâmpada elétrica, ela se acenderá.
5. Os elétrons que chegam à barra de cobre se unem aos íons Cu2+ da solução, reduzindo-os e transformando-os em cobre metálico. O eletrodo em que ocorre a redução é o catodo, ou polo positivo.
6. Um tubo contendo uma solução de sal une as cubas com as duas soluções. Essa ponte salina tem a finalidade de neutralizar as duas soluções em torno dos eletrodos – ou seja, equilibrar o excesso de íons de zinco, de um lado, e a falta de íons de cobre, de outro lado.
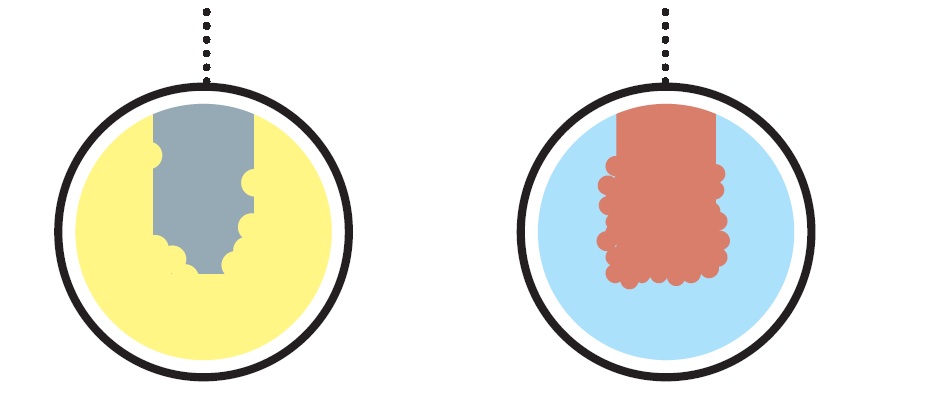
7. Com o tempo, a lâmina de zinco oxidada sofre corrosão e perde massa. No cátodo, por outro lado, a redução faz com que cada vez mais cobre metálico se prenda à superfície da barra, que ganha massa.
O QUE ISSO TEM A VER COM FÍSICA
O que ocorre no interior de uma pilha ou bateria tem a ver com conversão de energia. Esses dispositivos, tratados na física como geradores, transformam a energia química das substâncias em seu interior em energia elétrica. Essa eletricidade é conduzida até um receptor, que fará nova conversão, agora da eletricidade para outra modalidade de energia – mecânica (movimento das lâminas de um liquidificador), térmica (aquecimento do chuveiro elétrico) ou radiante (acendendo os faróis de um veículo).
Potência de uma pilha
A potência de uma pilha é a facilidade com que ocorre a transferência de elétrons de um eletrodo a outro. Os químicos construíram uma escala de potenciais-padrão de redução e de oxidação (E0red ou E0ox), que são medidos em volts (V). A escala é baseada no hidrogênio, a que foi atribuído potencial-padrão zero. Todas as substâncias são comparadas ao hidrogênio. Ao comparar duas espécies, a de maior E0 red recebe elétrons, e a de menor doa elétrons.

Entenda a tabela:
- Todo material com E0 red negativo tem menor potencial que o hidrogênio de sofrer redução. São espécies químicas que tendem a doar elétrons ao íon H+.
- Os materiais com E0 red positivo têm maior potencial que o hidrogênio de sofrer redução. Tendem a receber elétrons de H2.
- O potencial de oxidação de um material tem o mesmo valor que seu potencial de redução, só que com o sinal invertido. Por exemplo:
Potencial de redução: Zn2+ (aq) + 2 e– → Zn(s) E0 = – 0,76 V
Potencial de oxidação: Zn(s) → Zn2+ (aq) + 2 e– E0ox = + 0,76 V
Quanto maior for a diferença de potencial de redução de duas espécies químicas, maior será a capacidade dessas substâncias de doar e receber elétrons em uma pilha. Para calcular essa diferença de potencial (ΔE), somamos o potencial de redução da espécie que sofre redução ao potencial de oxidação da espécie que sofreu oxidação. No caso do zinco e do cobre:
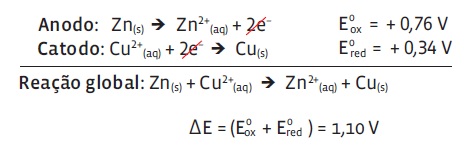
Espontaneidade da reação
É bom lembrar que todas as pilhas funcionam por reações espontâneas e apresentam sempre um ΔE positivo (ΔE > 0). Veja como se avalia a espontaneidade de uma reação:
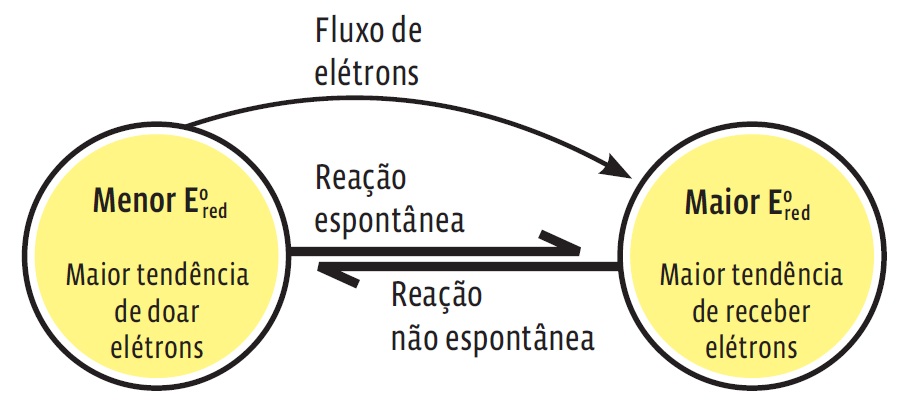
Como escrever a equação global de uma pilha:
• Escreva a semirreação no sentido da redução e copie o valor de E0red;
• Escreva a semirreação no sentido da oxidação e inverta o sinal do valor de E0red;
• Se necessário, multiplique as equações para igualar o número de elétrons cedidos ao número de elétrons recebidos;
• O valor do potencial-padrão dos eletrodos não deve ser multiplicado, pois não depende da quantidade de elétrons doados ou recebidos;
• Por fim, some as equações para obter a reação global.
EQUAÇÃO GLOBAL
Monte a equação da pilha formada por eletrodos de cobre (Cu) e prata (Ag), dados os potenciais-padrão de redução abaixo:
Cu2+(aq) + 2 e– → Cu(s) Ered = + 0,34 V
Ag+(aq) + e– → Ag(s) Ered = + 0,80 V
- • Das duas substâncias, Cu2+(aq) tem o menor potencial de redução – sofre oxidação. Já Ag+(aq) tem maior potencial de redução – sofre redução.
- • A semirreação do cobre no sentido da oxidação é:
Cu (s → Cu2+(aq) + 2 e– Eox = – 0,34 V
- • A semirreação da prata no sentido da redução é:
Ag+(aq) + e– Ω Ag(s) Ered = + 0,80 V
- • Multiplicamos a reação de redução da prata por 2 para igualar o número de elétrons recebidos ao número de elétrons doados:
2 Ag+(aq) + 2 e– Ω 2 Ag(s) Ered = + 0,80 V
- • Somando as equações:
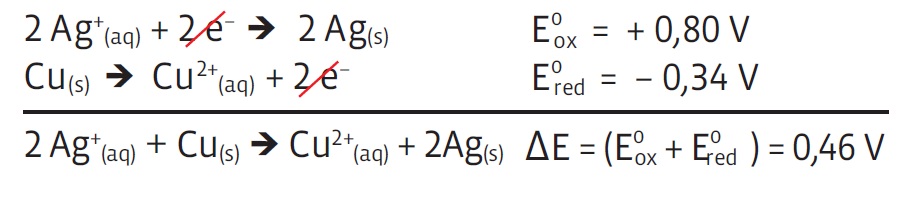
- Esta é a equação da reação global pedida.










