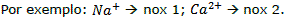Óxido-redução
Compartilhe essa matéria: Link copiado! Reações em que os elementos ganham ou perdem elétrons são chamadas de reações de óxido-redução. Obs.: Apesar das aparências, não só as reações envolvendo substâncias iônicas implicam em troca de elétrons. 1. Número de oxidação (nox): é o número de elétrons que um átomo ganha ou perde em uma reação […]
Reações em que os elementos ganham ou perdem elétrons são chamadas de reações de óxido-redução.
Obs.: Apesar das aparências, não só as reações envolvendo substâncias iônicas implicam em troca de elétrons.
1. Número de oxidação (nox): é o número de elétrons que um átomo ganha ou perde em uma reação de óxido-redução. Se o átomo ganha elétrons seu nox será negativo; se perde será positivo.

2. Regras para determinação do nox: essas regras ajudam a entender as relações de ganhos e perdas de elétrons em uma reação de óxido-redução.
a. o nox de um cátion ou de um ânion é igual a própria carga.
b. a soma dos nox de um composto é sempre igual a zero. 
c. substâncias simples apresentam nox igual a zero. 
d. existem elementos que possuem nox definidos: 
e. o nox dos halogênios (F, Cl, Br, I, At) é -1. 
f. o nox do hidrogênio em substâncias compostas é, geralmente, +1. 
g. o nox do oxigênio será -2, em geral.
3. Classificação das reações e dos agentes em reações de óxido-redução: se houver uma perda de elétrons a reação será chamada de reação de oxidação; quando há ganho de elétrons é chamada de reação de redução.
O elemento que sofre oxidação é chamado de agente redutor e o que sofre redução é chamado de agente oxidante.

4. Balanceamento de equações de óxido-redução: a regra é que o número de elétrons perdidos seja igual ao número de elétrons ganhos. 
Embora a quantidade de elementos está balanceada o número de elétrons não está. Há um núcleo de alumínio no primeiro membro da reação e um de cobre no segundo; porém, enquanto o cobre recebe 2 elétrons passando de nox +2 para 0, o alumínio perde 3 elétrons passando de nox 0 para nox +3. Para balancear a equação e igualar o número de elétrons perdidos e ganhos devemos multiplicar os alumínios por 2 e os cobres por 3 em ambos os lados, ficando a equação, então: 
Exercícios:
1.
a. +3 e +6.
b. +2 e +4.
c. +2 e +2.
d. zero e +4.
e. zero e +2.
2. (Vunesp-SP) No mineral perovsquita, de fórmu¬la mínima CaTiO3, o número de oxidação do titânio é:
a. +4.
b. +2.
c. +1.
d. -1.
e. -2.
3. (UFV-MG) No processo de obtenção do aço, ocorre a reação representada por:

I – Qual elemento sofre redução?
II— Qual elemento sofre oxidação?
III – Qual substância é o agente redutor?
IV – Qual substância é o agente oxidante?
V – Acerte os coeficientes da equação.
4. (Cesgranrio-RJ) Dada a equação:

os coeficientes, na ordem em que aparecem após o balanceamento, são:
a. 1; 4; 2; 1; 2; 2.
b. 1; 4; 1; 1; 1; 2.
c. 2; 4; 2; 2; 2; 2.
d. 1; 2; 1; 1; 1; 2.
e. 2; 4; 1; 2; 1; 4.
Respostas:
1. b.
2. a.
3.
I – ferro.
II – carbono.
III – monóxido de carbono.
IV – óxido de ferro
V – 
4. b.
 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO